Spasticity is a velocity dependent increase in resistance to stretch and is a common sign of upper motor neuron disorder that is seen in conditions such as stroke, multiple sclerosis (MS), cerebral palsy (CP), and brain injury. When untreated, spasticity in some patients can result in pain, deformity, impaired functional abilityReference Shaw, Rodgers and Price 1 , Reference Ward, Aguilar and De Beyl 2 , and significantly impact the quality of life. Botulinum toxin type-A (BoNTA) presynaptically blocks transmission at the neuromuscular junctionReference Turkel, Bowen, Liu and Brin 3 and is regarded as an effective treatment option for the management of focal spasticity. Delivered by intramuscular injection into the affected muscle, BoNTA causes local and temporary paresis of the muscle and may also provide an analgesic effect lasting for three to four monthsReference Shaw, Rodgers and Price 1 . Therefore, decrease in spasticity with BoNTA has the potential to improve range of motion, function, and participation in activities of daily living.
In addition to spasticity, BoNTA is also used for a variety of disorders and conditions involving injections in various body partsReference Truong, Stenner and Reichel 4 and is also increasingly being used for cosmetic improvementsReference Truong, Stenner and Reichel 4 . Although BoNTA is accepted as safe for therapeutic use, both local and systemic adverse events (AEs) have been reported in the literature 5 , Reference Merz 6 . Reported AEs related to BoNTA include the symptoms in different systems such as musculoskeletal (pain and weakness), neurologic, visual, oropharyngeal, respiratory, immune system, bowel and bladder, cardiovascular, resulting in extreme cases in anaphylaxis, and spontaneous death 5 - Reference Roche, Schnitzler, Genet, Durand and Bensmail 7 . However, these AEs were reported for a variety of conditions and not specifically for spasticityReference Coté, Mohan, Polder, Walton and Braun 8 .
Botulinum toxin type-A use for spasticity management may differ from that used for other conditions. Intramuscular injections for spasticity management are administered into skeletal muscles that can vary in size ranging from the small foot and hand muscles to large muscles such as quadriceps and gastro-soleus complex and may require injections in multiple sites in the same muscle. The unique sites for BoNTA injections into muscles with spasticity and features of the intramuscular injections specific to spasticity management are likely to result in AEs that differ from those experienced in the management of other conditions (visual problems, dystonia, and cosmetic purposes). Furthermore, the total dose injected in patients with spasticity is generally higher than other conditions. Currently, there are no data summarizing the AEs of BoNTA when used for spasticity management.
The knowledge of AEs specific to the BoNTA injections used to manage spasticity will assist physicians to make informed decisions and guide more effective management of spasticity. The purpose of this study was to investigate the AEs of BoNTA for spasticity management reported in Canada and in the medical literature. Specifically, we wanted to determine a) the most common AEs following BoNTA treatment for spasticity – a1) number and type of AEs reported to the federal drug regulation agency in Canada, a2) and in scientific literature, and b) the parameters of BoNTA treatment (such as type of toxin used, dosage, location of injection, diagnoses) associated with the AEs.
Methods
Health Canada is a federal department in Canada that maintains records of AEs of drugs including BoNTA reported by health care providers, pharmacists, or consumers. We requested Health Canada to provide us with details of AEs reported to Health Canada from 2009 to 2013 for intramuscular BoNTA injections (onabotulinumtoxinA and incobotulinumtoxinA) for spasticity. IncobotulinumtoxinA was approved for focal spasticity in upper limbs only in Canada in 2009 (much later than onabotulinumtoxinA approved in 2001 for spasticity in both upper and lower limbs 9 ) and hence we sought the data beginning from the year 2009. These are the two toxins that have received approval in Canada for the management of spasticity.
Data were compiled into sub-categories for descriptive analyses. The following categories were used to describe the data: a) Muscle AEs: hypotonia, asthenia, hypokinesia, abasia, and dysstasia; b) Oropharyngeal AEs: dysarthria, dysphagia, pharyngitis, feeding disorder, speech disorder, tongue paralysis, mastication disorder, altered saliva production, dysphonia, laryngospasm, vocal cord disorder, trismus, drooling, ageusia, stomatitis, aphagia, dry mouth, oral swelling, oral pain, tongue hemorrhage, tooth ache, slow speech, and eating disorder; c) Respiratory AEs – dyspnoea, cough, increased respiratory rate, pulmonary artery aneurysm, pulmonary embolism, choking, pneumonia, broncho-pneumonia, abnormal chest x-ray, diaphragmatic weakness and paralysis, aspiration pneumonia, mechanical ventilation, tracheostomy, asphyxia, pleural effusion, bronchospasm, chest pain, lung disorder, pulmonary fibrosis, crepitation and respiratory distress, metastases to lung, asthma; d) Eye related AEs: eyelid ptosis, abnormal pupillary light tests, blepharospasm, eyelid oedema, dry eye, eye swelling, photophobia, strabismus, visual impairment, vision blurred, diplopia, eye pruritus, ocular hyperaemia, eyelid function disorder, visual acuity reduced, excessive eye blinking; e) Bowel/Bladder AEs: constipation, nausea, vomiting, decreased appetite, intestinal ischemia, small intestinal obstruction, recto sigmoid cancer, fecal incontinence, gastrointestinal motility disorder, colon cancer, urinary incontinence and urinary retention, dysuria, hematuria, pollakiuria, urosepsis, bladder spasm, and urinary tract infection; f) Infection AEs: flu-like symptoms, streptococcal, pyrexia, chills, sepsis, and septic shock.
Systematic review search strategy
PubMed, EMBASE, CINAHL, and PEDro databases were searched using the key word combinations below (Figure 1). The keywords were selected from literature reviews and botulinum toxin type A drug monographs 5 , Reference Merz 6 that listed the AEs occurring from treatment with BoNTA. These keywords were then searched on PubMed to create a list of parallel medical subject headings (MeSH) terms. The key word combinations used in the database searches were aimed at increasing the likelihood of finding relevant articles. Additionally, the reference lists of relevant articles were searched to find more sources. These MeSH terms were reported in product monographs (for Botox – onabotulinumtoxinA and Xeomin – incobotulinumtoxinA; approved for use in Canada) as AEs of BoNTA.
MeSH term combinations
The MeSH terms botulinum toxins, type A and muscle spasticity were combined with the MeSH terms and key words as shown in Figure 1. These side effects are reported in product monographs (for onabotulinumtoxinA 5 and incobotulinumtoxinAReference Merz 6 ) as adverse effects of BoNTA.
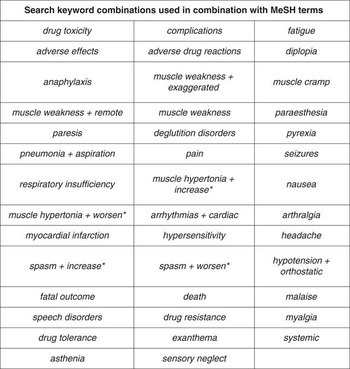
Figure 1 MeSH terms and key words combined with MeSH terms botulinum toxins, type A and muscle spasticity.
Study selection
After performing the initial database search, two authors (AH and CD) scanned the titles and abstracts of the papers for relevance. Research papers were considered relevant if they discussed AEs of BoNTA for the treatment of spasticity in adults. The etiology of spasticity included in this review was broad and included stroke, MS, spinal cord injury (SCI), and CP. Systematic reviews were not included in this study but their reference lists were scanned for relevant articles. Once the databases had been searched and reviewed for relevance, the full texts of the remaining articles were procured by the investigators. The articles used in the review were subject to the following inclusion criteria: 1) English language publications, 2) human studies, 3) adult subjects (age >18 years), 4) publications from 1990 to 2013, 5) studies that used botulinum toxin type-A, 6) studies that investigated spasticity treatment, 7) studies that reported AEs. The two authors (AH and CD) mutually agreed to include or exclude the articles from the literature search based on the above criteria. If articles were found to not be relevant upon reading the full text, they were excluded.
Data extraction
Based on the above criteria, relevant articles were chosen and their results were extracted. Data such as the author, year of publication, type of AE experienced, diagnosis, brand and dose of toxin used, proportion of patients experiencing the AE, location of injection, and guidance technique were compiled into tables. The Oxford Centre for Evidence-Based Medicine (2011) levels of evidenceReference Howick, Chalmers and Library 10 were used to grade the quality of the articles. Each article was graded independently by two authors (AH and CD) and then compared. If there were any discrepancies, they were resolved through discussion and a level of evidence was agreed upon.
Results
Sources of AE data
For onabotulinumtoxinA: 34 reports (12%) came from community setting, 231 reports (85%) came from market authorization holder (manufacturer), and 7 reports (3%) from hospital setting. Overall consumers reported 42 events (15%) whereas clinicians or healthcare professionals reported 230 events (85%). For incobotulinumtoxinA: 1 report (8%) was from community setting and 12 reports (92%) came from market authorization holder. Clinicians or healthcare professionals reported 10 events (77%) and consumers reported 3 events (23%).
Canada adverse events
A total of 285 reports of AEs were made to Health Canada between 2009 – 2013; of which 272 reports were for onabotulinumtoxinA and 13 for incobotulinumtoxinA.
OnabotulinumtoxinA
Out of all reported events (n=272; one event refers to one AE reported in one patient, mean age 48±19 years; See Figure 2), 68% were reported in females, 53% were reported to be serious, 18% required hospitalization, and 8% resulted in death. The type of AEs reported were: muscle weakness (19%), oropharyngeal AEs (14%), respiratory AEs (14%), eye AEs (8%), bowel/bladder AEs (8%), and infection related AEs (5%).

Figure 2 Categories of adverse events as a percentage of total adverse events with onabotulinumtoxinA reported to Health Canada. (Note: Data from incobotulinumtoxinA is not reported here because of insufficient AE data to allow comparison with onabotulinumtoxinA.)
IncobotulinumtoxinA
Out of all reported events (n=13; mean age 59±15 years), 38% were reported in females, 62% were serious, 54% required hospitalization, but none resulted in death. The type of AEs reported were: muscle weakness (15%), oropharyngeal AEs (15%), respiratory AEs (38%), and eye related AEs (23%), bowel/bladder AEs (15%), and infection related AEs (15%).
In the onabotulinumtoxinA group, 33% cases, (out of the 125 cases where the dose was reported), received >360 units of BoNTA (approved maximum cumulative dose in Canada 5 ). In the incobotulinumtoxinA group, none of the 13 cases received more than 400 units of BoNTA (approved maximum cumulative dose in CanadaReference Merz 6 ). Data such as guidance technique used and type of upper motor neuron lesion were not available from Health Canada. Although not an adverse event, ineffectiveness of the toxin (44% onabotulinumtoxinA and 23% incobotulinumtoxinA) was one of the categories of information in the Health Canada data.
Systematic review of worldwide adverse events
The original search of the PubMed, EMBASE, CINAHL, and PEDro databases yielded 1346 articles (see Figure 3) and 50 articles were found to be relevant to the study topic. After a review of the full texts of these articles, 29 met the inclusion criteria and were included in this systematic review. Ten of these studies represented a high level of evidence (level 2). Nine studies were graded level 3 and the remaining ten were graded level 4 (see Tables 1, 2, 3). The total number of patients injected across the 29 studies was 2467; of this, 801 patients (32%) experienced AEs.

Figure 3 PRISMA 2009 Flow Diagram From: Moher D, Liberati A, Tetzlaff J, Altman DG, The PRISMA Group (2009). Preferred Reporting Items for Systematic Reviews: The PRISMA Statement. PLoS Med 6(6): e1000097. doi:10.1371/journal.pmed1000097 For more information, visit www.prisma-statement.org
Table 1 Adverse events in studies reporting use of onabotulinumtoxinA

MS-multiple sclerosis; CP-cerebral palsy; TBI-traumatic brain injury; SCI-spinal cord injury; ALS-amyotrophic lateral sclerosis; LOE-level of evidence (Oxford); UE-upper extremity; LE-lower extremity; EMG-electromyography; NA-not available; CT-computerized tomography; CK-creatine kinase; UTI-urinary tract infection
Table 2 Adverse events in studies reporting use of abobotulinumtoxinA

CK-creatine kinase; UTI-urinary tract infection; TBI-traumatic brain injury
MS-multiple sclerosis; CP-cerebral palsy; TBI-traumatic brain injury; SCI-spinal cord injury; ALS-amyotrophic lateral sclerosis; LOE-level of evidence (Oxford); UE-upper extremity; LE-lower extremity; EMG-electromyography; NA-not available; UTI-urinary tract infection
Table 3 Adverse events in studies reporting use of incobotulinumtoxinA

MS-multiple sclerosis; CP-cerebral palsy; LOE-level of evidence (Oxford); UE-upper extremity; EMG-electromyography
AEs such as muscle weakness,Reference Turkel, Bowen, Liu and Brin 3 , Reference Roche, Schnitzler, Genet, Durand and Bensmail 7 , Reference Muller, Cugy and Ducerf 11 - Reference Pullman, Greene, Fahn and Pedersen 29 hypertoniaReference Turkel, Bowen, Liu and Brin 3 , Reference Gusev, Banach and Simonow 17 , Reference Gordon, Brashear and Elovic 21 , Reference Hyman, Barnes and Bhakta 25 and other muscle related AEs such as cramps, incoordination, stiffness, general motor dysfunctionReference Turkel, Bowen, Liu and Brin 3 , Reference Roche, Schnitzler, Genet, Durand and Bensmail 7 , Reference Muller, Cugy and Ducerf 11 , Reference Gordon, Brashear and Elovic 21 were reported in 20 studies reviewed here. Injection site pain was reported in eight studiesReference Turkel, Bowen, Liu and Brin 3 , Reference Muller, Cugy and Ducerf 11 , Reference Barnes, Schnitzler, Medeiros, Aguilar, Lehnert-Batar and Minnasch 19 , Reference Gordon, Brashear and Elovic 21 , Reference Mohammadi, Balouch, Dengler and Kollewe 28 - Reference Kanovsky, Slawek and Denes 31 and non-injection site related pain (arthralgia, headache, myalgia, and abdominal and back pain) was also reported in twelve studiesReference Shaw, Rodgers and Price 1 , Reference Turkel, Bowen, Liu and Brin 3 , Reference Muller, Cugy and Ducerf 11 , Reference Gusev, Banach and Simonow 17 , Reference Simpson, Gracies, Yablon, Barbano, Brashear and Team 18 , Reference Gordon, Brashear and Elovic 21 - Reference Pittock, Moore and Hardiman 23 , Reference Hyman, Barnes and Bhakta 25 , Reference Kaji, Osako and Suyama 32 , Reference Kanovský, Slawek and Denes 33 . Furthermore, oropharyngeal AEs (dysphagia, dry mouth, pharyngitis, dysarthria, recurrent choking, and dysphonia) were reported in seven studiesReference Bakheit, Ward and McLellan 14 , Reference Crowner, Torres-Russotto, Carter and Racette 16 , Reference Gusev, Banach and Simonow 17 , Reference Pittock, Moore and Hardiman 23 , Reference Coban, Matur, Hanagasi and Parman 24 , Reference Bakheit, Fedorova, Skoromets, Timerbaeva, Bhakta and Coxon 30 , Reference Kanovsky, Slawek and Denes 31 and bowel and bladder AEs were reported in six studiesReference Shaw, Rodgers and Price 1 , Reference Crowner, Torres-Russotto, Carter and Racette 16 , Reference Gordon, Brashear and Elovic 21 , Reference Hyman, Barnes and Bhakta 25 , Reference Kanovský, Slawek and Denes 33 , Reference Bruggemann, Dognitz, Harms, Moser and Hagenah 34 . Circulation related AEs (peripheral edema, contusion/hematoma, hypertension, postural hypotension, erectile dysfunction, paleness) were reported in nine studiesReference Turkel, Bowen, Liu and Brin 3 , Reference Muller, Cugy and Ducerf 11 , Reference Barnes, Schnitzler, Medeiros, Aguilar, Lehnert-Batar and Minnasch 19 , Reference Gordon, Brashear and Elovic 21 , Reference Kanovsky, Slawek and Denes 31 - Reference Papadonikolakis, Vekris, Kostas, Korompilias and Soucacos 35 .
Neurologic AEs (epilepsy, seizure, convulsions, dystonia, paraesthesia, and hyperaesthesia)Reference Turkel, Bowen, Liu and Brin 3 , Reference Muller, Cugy and Ducerf 11 , Reference Crowner, Torres-Russotto, Carter and Racette 16 , Reference Gordon, Brashear and Elovic 21 , Reference Pittock, Moore and Hardiman 23 , Reference Suputtitada and Suwanwela 26 , Reference Kanovský, Slawek and Denes 33 and gait abnormalities and falls were reported in seven studies eachReference Shaw, Rodgers and Price 1 , Reference Crowner, Torres-Russotto, Carter and Racette 16 , Reference Simpson, Gracies, Yablon, Barbano, Brashear and Team 18 , Reference Joshi 20 , Reference Pittock, Moore and Hardiman 23 , Reference Hyman, Barnes and Bhakta 25 , Reference Kaji, Osako and Suyama 32 . Infection related AEs (flu like symptoms, abscess, infection, fever) were reported in five studiesReference Shaw, Rodgers and Price 1 , Reference Joshi 20 , Reference Hyman, Barnes and Bhakta 25 , Reference Dunne, Heye and Dunne 27 , Reference Opara, Hordyńska and Swoboda 36 . Respiratory AEs (cough, dyspnoea, respiratory distress, upper respiratory tract infection, chest infection, and orthopnea) were reported in six studiesReference Shaw, Rodgers and Price 1 , Reference Turkel, Bowen, Liu and Brin 3 , Reference Crowner, Torres-Russotto, Carter and Racette 16 , Reference Coban, Matur, Hanagasi and Parman 24 , Reference Hyman, Barnes and Bhakta 25 , Reference Kanovsky, Slawek and Denes 31 . General AEs (mild discomfort, dizziness, nausea, tooth disorder, somnolence, insomnia, and altered blood test results) were reported in eleven studiesReference Shaw, Rodgers and Price 1 , Reference Turkel, Bowen, Liu and Brin 3 , Reference Simpson, Gracies, Yablon, Barbano, Brashear and Team 18 , Reference Barnes, Schnitzler, Medeiros, Aguilar, Lehnert-Batar and Minnasch 19 , Reference Gordon, Brashear and Elovic 21 - Reference Pittock, Moore and Hardiman 23 , Reference Hyman, Barnes and Bhakta 25 , Reference Dunne, Heye and Dunne 27 , Reference Kaji, Osako and Suyama 32 , Reference Kanovský, Slawek and Denes 33 . Eye related AEs (diplopia, difficulty keeping eyes open, ptosis) were reported in three studiesReference Roche, Schnitzler, Genet, Durand and Bensmail 7 , Reference Bakheit, Ward and McLellan 14 , Reference Crowner, Torres-Russotto, Carter and Racette 16 .
Botulinum toxin type-A dosage injected in the studies included in this review varied widely – ranging from 10 – 800 units (onabotulinumtoxinA), 100 – 1500 units (Dysport - abobotulinumtoxinA), and 300 – 400 units (incobotulinumtoxinA). OnabotulinumtoxinA was used in thirteen, abobotulinumtoxinA in nine studies and incobotulinumtoxinA in three studies as the type of BoNTA toxin administered for spasticity treatment. Finally, four studies used a combination of both abobotulinumtoxinA and onabotulinumtoxinA as the BoNTA toxins for spasticity management.
The most commonly reported diagnosis where BoNTA was administered resulting in any AE was stroke in eighteen studies followed by MS in seven studies. Brain injury and CP were each the diagnoses in two of the studies and other less common diagnoses are reported in Tables 1, 2, and 3. Each of these diagnoses was reported in a combination or alone in one study reviewed. The BoNTA injection location was evenly distributed between upper extremity (34%), lower extremity (31%), and combined upper and lower extremity injection studies (31%).
Guidance technique: 17 studies used electromyography or electrical stimulation to localize the site of injections whereas 12 studies either used no guidance or used localization of anatomical landmarks and palpation.
Discussion
While AEs are routinely reported in the research studies and clinical trials using BoNTA treatments for a variety of indications, our study reports the data specific to spasticity. An in-depth understanding of possible AEs and the underlying mechanisms can help clinicians account for these potential AEs and manage spasticity effectively. These AEs can be explained by: (1) the local AEs of BoNTA; (2) the systemic effects from spread of the toxin to surrounding and remote areas via two possible routes. Systemic effects can be further explained by either a vascular spread or a retrograde axonal spread.
Local adverse events of BoNTA administration
Muscle related AEs such as weakness limited to the vicinity of the injected muscles was the second most common AE in Canada and the most commonly reported AE in the majority of the studies reviewed here. Muscle weakness can be attributed to the administration of excess quantity of toxinReference Hecht, Stolze and Auf dem Brinke 22 , Reference Hyman, Barnes and Bhakta 25 , Reference Lange, Brin, Warner, Fahn and Lovelace 37 , Reference Naidu, Smith, Sheedy, Adair, Yu and Graham 38 resulting in acute and severe muscle paresis. Local muscle atrophyReference Bakheit, Ward and McLellan 14 is proposed to result from continued blockade of neurotransmissionReference Joshi 20 causing effects similar to anatomic denervationReference Ghasemi, Salari, Khorvash and Shaygannejad 39 . In animal models, botulinum toxin has been shown to spread to muscles in the same compartment as the injected muscleReference Yucesoy, Emre Arıkan and Ateş 40 . The local spread of the toxin to nearby muscles within the same compartment can weaken the muscles and can contribute to decrease in force outputReference Yucesoy, Emre Arıkan and Ateş 40 . It has been suggested that total toxin injected in muscles throughout the body may increase weaknessReference Brin, Lyons and Doucette 41 , whereas others contest this viewReference Muller, Cugy and Ducerf 11 . Though considered reversibleReference Muller, Cugy and Ducerf 11 , Reference Joshi 20 , severe acute local weakness of the injected muscle can be counterproductive because it can lead to muscle imbalance and further loss of functionReference Roche, Schnitzler, Genet, Durand and Bensmail 7 .
Although dosage guidelines exist in treating children with spasticityReference Naidu, Smith, Sheedy, Adair, Yu and Graham 38 , Reference Heinen, Molenaers and Fairhurst 42 , similar guidelines are missing for treatment with BoNTA in adults with spasticityReference Wissel, Ward and Erztgaard 43 . Lack of clarity and consensus regarding dose can lead to physicians injecting too little or too much toxin when spasticity management with BoNTA is first initiated. Clear guidelines can prevent unwanted and serious AEs, give practical guidance regarding upper limits of BoNTA dose and change practice of BoNTA injectionsReference Naidu, Smith, Sheedy, Adair, Yu and Graham 38 . In addition, not all types of neurological lesions experience similar levels of spasticity across the limbs and may require different overall doses depending on the spasticity manifestation patternReference Phadke, Davidson, Ismail and Boulias 44 . Studies reporting doses in individual muscles and limbs across a variety of neurological lesions are emergingReference Phadke, Davidson, Ismail and Boulias 44 , Reference Esquenazi, Mayer and Lee 45 and will help guide physicians regarding dosages used by other practitioners.
While low doses can result in ineffectiveness of the toxin, high doses can potentially increase the AEsReference Caleo, Antonucci, Restani and Mazzocchio 46 - Reference Kaji, Osako and Suyama 48 . One third (33%) of the patients receiving onabotulinumtoxinA received doses greater than the maximal cumulative dose recommended in the product monograph. In the studies reviewed here, 7/17 studies (41%) injected greater than 360 units of onabotulinumtoxinA, 7/13 studies (54%) injected greater than 1000 units (maximum recommended cumulative dose 49 ) of abobotulinumtoxinA, and none of the studies exceeded the maximal cumulative dose recommended in the product monograph for incobotulinumtoxinA. Thus, it is possible that high dose may be one of the factors underlying muscle weakness. Some studies in this systematic review also reported hypertonia as an AE. It has been suggested that hypertonia may not be in response to BoNTA but rather a normal variation in toneReference Hyman, Barnes and Bhakta 25 in response to various environmental factorsReference Phadke, Balasubramanian, Ismail and Boulias 50 . Additionally, another factor contributing to hypertonia may be the unmasking of underlying spasticity post-BoNTA injections in adjacent and/or synergistic uninjected muscles in response to reduction of spasticity in injected musclesReference Gusev, Banach and Simonow 17 .
Injection site pain was not reported as an AE in Canada in spite of several studies reviewed in the literature reporting this AE. A possible reason injection site pain was not reported to Health Canada was because pain is expected during a procedure such as repetitive intramuscular BoNTA injectionsReference Gordon, Brashear and Elovic 21 . Application of ice packs is known to decrease BoNTA injection related painReference Fung, Phadke, Kam, Ismail and Boulias 51 and ice packs may have a more therapeutic role in managing local injection related pain. Pain and other local injection site AEs such as bruising, burning, and hypersensitivity may be preventable in some instances by exercising caution in the technique of injecting BoNTAReference Kaji, Osako and Suyama 32 . One study reported higher frequency of AEs in the BoNTA groupReference Gusev, Banach and Simonow 17 but, it should be noted, some placebo-controlled studies report similar frequency of treatment related AEs in the BoNTA and the placebo groupsReference Shaw, Rodgers and Price 1 , Reference Turkel, Bowen, Liu and Brin 3 , Reference Hyman, Barnes and Bhakta 25 , Reference Kanovsky, Slawek and Denes 31 , Reference Kaji, Osako and Suyama 32 , Reference Kaji, Osako and Suyama 48 . It is possible that at least some of the AEs may be related to injection technique. Close to half (41%) of the studies included in this review either used no guidance or anatomical landmarks and palpation and none of the studies used ultrasound guidance. It is possible that lack of precision during injections as afforded by electromyelography (EMG) and electrical stimulationReference Chin, Nattrass, Selber and Graham 52 may be a contributing factor towards some of the AEs. Other local AEs such as skin reactions (e.g., rash) have been attributed to allergic responsesReference Bruggemann, Dognitz, Harms, Moser and Hagenah 34 to the toxin; however, such minor AEs are less common.
Seven studies included in this review reported non-injection site related pain (e.g. myalgia and headache) as an AE. In all these studies, BoNTA injections were predominantly delivered in the upper limbs; however, it is not clear what factors may have resulted in AEs such as headache and myalgia. Paradoxically, BoNTA has been used to treat myalgia in upper extremityReference Wendel and Cole 53 and thus, the mechanism underlying AEs such as myalgia and headache after BoNTA injections is unclear. Botulinum toxin type-A is typically injected in multiple muscles and multiple sites within a muscle. It is possible that multiple injection sites caused bruising and the cumulative effect was seen in the form of myalgia. Hands are known to have significantly larger sensory cortical representation than legs and four out of seven studies reporting pain involved injections in hand muscles. It is possible that multiple injections in the hand area may be responsible for myalgia. Presentation of headache may be a result of systemic effects of BoNTA.
Systemic adverse events of BoNTA
Relatively serious AEs in association with BoNTA including hospitalization, or fatality, have also been reported in addition to AEs in categories like oropharyngeal, respiratory, eyes, bowel/bladder, and infection. Mechanisms underlying some of these AEs have been proposed but conclusive evidence is lacking. Two possible systems of spread (vascular and retrograde axonal spread) have been suggested in the literatureReference Garner, Straube, Witt, Gasser and Oertel 54 .
a) Vascular spread: Direct administration into blood circulation is unlikely because typically needles are aspirated for blood before injections; however, the distant AEs of BoNTA suggest that vascular spread is possible through means other than direct administration into the blood stream. Botulinum toxin type-A can induce autonomic effects such as biliary colic and impact the gastrointestinal autonomic pathwaysReference Schnider, Brichta, Schmied and Auff 55 , impair the cardiovascular autonomic pathwaysReference Girlanda, Vita, Nicolosi, Milone and Messina 56 , and inhibit autonomic cholinergic pathways in the bladderReference MacKenzie, Burnstock and Dolly 57 . Although it is difficult to imagine a direct link between the respiratory and immunity related AEs of BoNTA, other factors may indirectly be responsible. Cholinergic receptors in the pharyngeal and laryngeal sphincters are likely to be inhibited by systemic spread of BoNTA and may be the primary reason for dysphagia/dysphonia. Additionally, incoordination of the laryngeal and pharyngeal sphincter activity can compromise airway protection and make patients vulnerable to aspiration of oral and esophageal contentsReference Naidu, Smith, Sheedy, Adair, Yu and Graham 38 , Reference Nigam and Nigam 58 . Aspiration may be one of the indirect mechanisms responsible for respiratory AEs and may also lead to possible immunity related AEs. One of the suggested mechanisms for transport of the toxin from one part of the body (neck) to a remote location (toes) is through the circulatory systemReference Lange, Brin, Warner, Fahn and Lovelace 37 . The short time interval between injection and onset of distant effects, in some cases within 24 hoursReference Naidu, Smith, Sheedy, Adair, Yu and Graham 38 , Reference Girlanda, Vita, Nicolosi, Milone and Messina 56 , also suggests that the toxin is transported systemically via vascular spread. Vascular spread via absorption through the capillary system remains a possibility. It is possible that a combination of both vascular and retrograde axonal spread of the toxin is responsible for distant AEsReference Papadonikolakis, Vekris, Kostas, Korompilias and Soucacos 35 , Reference Garner, Straube, Witt, Gasser and Oertel 54 .
For instance, Hyman in 2000Reference Hyman, Barnes and Bhakta 25 administered abobotulinumtoxinA to the hip adductor muscles of the upper thigh and postulated that the toxin could locally spread to the muscles around the pelvic floor, resulting in an increased incidence of urinary and fecal incontinence with BoNTA treatments. The relaxing anticholinergic effect of BoNTA on the striated and bladder wall muscles may be the underlying mechanism resulting in increased residual urineReference Naidu, Smith, Sheedy, Adair, Yu and Graham 38 , Reference Schnider, Berger, Schmied, Fertl and Auff 59 . Dysphagia, another serious AE, has been shown to occur in some patients. The close proximity of neck and proximal upper extremity muscles injected with BoNTA could result in the diffusion of the toxin into the surrounding muscles explaining the AE of dysphagiaReference Nigam and Nigam 58 , Reference Shaw and Rodgers 60 . However, three out of five studies reporting dysphagia as an AE injected the toxin in distant muscle groups, such as distal upper extremity muscle groups or even lower extremity muscle groups. Such a distant anticholinergic effect on the autonomic nervous system is unlikely through local spread of the toxin and a systemic spread has been suggested even when toxin is injected in sites anatomically adjacent to the locus of AEsReference Naidu, Smith, Sheedy, Adair, Yu and Graham 38 , Reference Girlanda, Vita, Nicolosi, Milone and Messina 56 .
Remote effects (muscle weakness): The weakness of muscles contralateral to the injected muscle was extremely rare and reported in very few studiesReference Thomas and Simpson 12 , Reference Varghese-Kroll and Elovic 13 , Reference Borg-Stein, Pine, Miller and Brin 15 . Local diffusion of the toxin through tissue planes and across the midline to the contralateral side is proposed as a mechanism for contralateral weaknessReference Thomas and Simpson 12 . Generalized weakness of muscles distant and remote to injection sites is much less common but nevertheless reported as an AE in some studiesReference Bakheit, Ward and McLellan 14 .
b) Retrograde axonal spread: Along with vascular systemic toxin spread, retrograde axoplasmic spread of the toxinReference Garner, Straube, Witt, Gasser and Oertel 54 , Reference Wiegand, Erdmann and Wellhöner 61 is the second possible mechanism for the observed distant AEs. Limited evidence exists in the literature based on human studies with evidence predominantly derived from animal studiesReference Caleo, Antonucci, Restani and Mazzocchio 46 . Based on a cat model, Wiegand (1976) demonstrated retrograde axonal transport of the toxin into the corresponding spinal cord segments using radioactive BoNTAReference Wiegand, Erdmann and Wellhöner 61 ; however, it was not clear if BoNTA remained enzymatically active after traveling into the spinal cord. More recent evidence shows retrograde transport of enzymatically active toxin molecules via microtubules in the axon to both sensory and motor regions in the spinal cord after intramuscular and intraneural injections of BoNTAReference Matak, Bach-Rojecky, Filipović and Lacković 62 , Reference Matak, Riederer and Lacković 63 . In fact, anti-nociceptive effect of BoNTA may occur through retrograde spread of BoNTA from the sensory nerves in the periphery to the central nervous systemReference Matak, Bach-Rojecky, Filipović and Lacković 62 . Additionally, BoNTA may share a similar time course as fast and long-range retrograde axonal transport to the central nervous systemReference Restani, Giribaldi and Manich 64 .
Lack of change in spinal reflex amplitude (H-reflexes) post-BoNTA has been suggested to refute the theory of retrograde axonal spreadReference Koman, Mooney, Smith, Walker and Leon 65 . However, both H-reflex and M-max (maximal motor response to electrical stimulation) are known to decrease after BoNTA and the ratio of Hmax/Mmax may not be an appropriate measure of central nervous system changeReference Phadke, Ismail and Boulias 66 . A better measure is reflex inhibition, and BoNTA injections have been reported to decrease recurrent or Renshaw-cell inhibition in persons post-strokeReference Caleo, Antonucci, Restani and Mazzocchio 46 , Reference Marchand-Pauvert, Aymard, Giboin, Dominici, Rossi and Mazzocchio 67 . Although both systemic vascular and axonal spread of the toxin is possible, the prolonged latency in appearance of some AEs such as the distant weakness is uncharacteristic of a mode of vascular toxin spread. Retrograde transport in such cases appears more likely. Thus, evidence points towards retrograde axonal uptake of the toxin and spread to the CNS and may be the underlying mechanism resulting in both distant muscular as well as the neurologic AEs seen in the studies included in this review. It should be noted however, that distant effects may also be in response to the intrafusal uptake of the toxin in the muscles spindles as well as neuroplastic changes post-BoNTA injectionsReference Caleo, Antonucci, Restani and Mazzocchio 46 , Reference Phadke, On, Kirazli, Ismail and Boulias 68 .
Preventable adverse events
It has been suggested that some of the AEs may be preventable. DoseReference Caleo, Antonucci, Restani and Mazzocchio 46 , Reference Nigam and Nigam 58 , Reference Borodic, Ferrante, Pearce and Smith 69 , injection techniqueReference Nigam and Nigam 58 and volumeReference Brodsky, Swope and Grimes 70 are some of the suggested preventable factors that can potentially affect distant spread of the toxin. Data from Canada shows that the most prevalent AE of BoNTA injections (onabotulinumtoxinA and incobotulinumtoxinA) was muscles weakness (range 15-19%); however, the percentage of oropharyngeal and respiratory problems (14-38%) among all AEs was much higher than pain (8-15%). With 33% cases with AEs receiving more than 360 units of onabotulinumtoxinA, it is possible that higher than typical dosesReference Phadke, Davidson, Ismail and Boulias 44 may be related to the AEs. It is also possible that some of the AEs of BoNTA injections are unrelated to the BoNTA treatment. Some patients treated with BoNTA may have pre-existing and co-morbid conditions such as seizure disordersReference Varghese-Kroll and Elovic 13 and in cases like these an AE of seizure can be better explained by the pre-existing condition rather than the effect of BoNTA injections. Minor AEs like minor falls, sitting imbalance, and minor gait abnormalities reported after BoNTA treatment may be related to the muscle weakness caused by the toxinReference Joshi 20 . For example, Pittock et al (2003) reported over-weakening of muscles with BoNTA injections resulting in a deterioration of the step length discrepancy observed in their patient populationReference Pittock, Moore and Hardiman 23 .
Non-responsiveness to treatment with BoNTA
Non-responsiveness to BoNTA could be as a result of a variety of factors reviewed elsewhereReference Benecke 71 . Possible factors include misdiagnosis, insufficient dose, first injection cycle placebo, problems with toxin storage and preparation, and administrationReference Joshi 20 , Reference Benecke 71 . Although 41% of the studies reviewed here either used no guidance or anatomical landmarks and palpation, we do not have information regarding guidance technique used to inject BoNTA in the AEs reported to Health Canada. Electrical stimulation, EMG, and ultrasound are well-established, precise, and beneficial guidance techniquesReference Walker, Lee, Bahroo, Hedera and Charles 72 . It is possible that use of imprecise guidance techniques such as palpation or anatomical landmarks alone may have resulted in problems with administration such as injecting the wrong muscle. Another possible reason for lack of clinical effect is immunoresistance to BoNTA, which refers to ineffectiveness of the toxin as a result of development of neutralizing antibodies against the toxinReference Benecke 71 . However, immunoresistance is reported to be very low with abobotulinumtoxinA (6.6%) in patients with spasticity and dystoniaReference Truong, Brodsky and Lew 73 and onabotulinumtoxinA (3%)Reference Anderson, Rivest and Stell 74 , Reference Zuber, Sebald, Bathien, de Recondo and Rondot 75 .
Serious adverse events
Data reported in this study represents events occurring across several countries. Of all AEs reported in Canada, 8% were deaths and this number was much lower than the 13% deaths reported among all AEs reported in USReference Coté, Mohan, Polder, Walton and Braun 8 . None of the studies included in this review reported death as an AE barring one where the deaths of study participants were unrelated to the toxinReference Turkel, Bowen, Liu and Brin 3 . The Health Canada data did not detail reasons for hospitalization (18% of all AEs) and the description of serious AEs (53% of all AEs). It is possible that some of the serious AEs may have been iatrogenicReference Coban, Matur, Hanagasi and Parman 24 ; however the presence of comorbidities can also partly explain some of the serious AEs. It should be noted that there was no indication from Health Canada data if there was a causal relationship between adverse events and toxin use.
Diversity of data
Out of the 29 articles reviewed, ten were from the United States of America (USA), five from the United Kingdom (UK) and the rest of the studies were from Germany (three), Turkey, Poland, Czech Republic, and France (two each), Japan, Thailand, and Greece (one each). Thus, in spite of a bias of studies in the USA and the UK, there was a reasonable representation from other countries barring the African and South American Continents.
Limitations
OnabotulinumtoxinA has been available for clinical use since the 1980s 76 and approved for upper or lower limb spasticity since 2001 9 ; whereas incobotulinumtoxinA has become available in Canada in 2009 77 . Additionally, onabotulinumtoxinA is approved for use in patients with focal spasticity in both upper and lower limbs 5 , whereas incobotulinumtoxinA is approved for use for spasticity in only upper limbs in patients with strokeReference Merz 6 . The differences in availability and approval for use (in addition to some differences in provincial formularies) can potentially explain the significantly fewer AEs with incobotulinumtoxinA. All these factors can play a role in the number and type of AEs and need to be taken into account when comparing the absolute numbers of AEs experienced with each preparation and interpreting the data.
Conclusions
Clinicians need to be aware of muscle weakness as a primary potential AE followed by oropharyngeal and respiratory problems associated with BoNTA injections for spasticity management. Mechanisms underlying these AEs need to be investigated using both animal and human models. Importantly, understanding the reasons for the AEs may assist in identifying risk factors and developing guidelines for minimizing occurrence of AEs with BoNTA treatments.
DISCLOSURES
Chetan Phadke has the following disclosure: Merz Pharma - Grant recipient; Farooq Ismail has the following disclosures: Allergan Inc. - Consultant, Honoraria/Speaker’s fees, Merz Pharma - Consultant, Honoraria/Speaker’s fees, Merz Pharma - Grant recipient, Grant support; Chris Boulias has the following disclosures: Allergan Inc. - Consultant, Honoraria, Merz Pharma - Consultant, Honoraria, Merz Pharma - Grant recipient, Grant; Chitra Balasubramanian, Alanna Holz, Caitlin Davidson do not have anything to disclose.







