Background
Autoimmune encephalidities are becoming an increasingly recognized cause of encephalitis, with a prevalence and incidence comparable to infectious encephalidities. Reference Dubey, Pittock and Kelly1 Autoimmune encephalidities (AIE) are thought to occur when there is an immune response directed against neuronal antigens either on the cell surface, at the synapse, or intraneuronally, all which lead to dysfunction of neurotransmission. Reference Van Coevorden-Hameete, De Graaff, Titulaer, Hoogenraad and Sillevis Smitt2 These include both paraneoplastic and non-paraneoplastic antibodies, which differ in treatment response and outcome. Reference Titulaer, McCracken and Gabilondo3,Reference Lancaster4 Much of the existing literature around AIE is focused on establishing the diagnosis and acute treatment, which includes corticosteroids, IVIg, plasma exchange and other immunotherapies. Reference Titulaer, McCracken and Gabilondo3–Reference Abboud, Probasco and Irani5 There is less information however, on chronic management of patients with AIE and long-term risk of relapse, especially for antibody negative AIE. Reference Titulaer, McCracken and Gabilondo3,Reference Lancaster4,Reference Lee, Lee and Kim6
Currently, there is equipoise in the need for steroid sparing immunotherapy after first attack, Reference Abboud, Probasco and Irani5 this is due to limited evidence, particularly for antibody negative AIE. Reference Abboud, Probasco and Irani5 Furthermore, there is lack of specific guidance regarding duration of immunotherapy after initial presentation and it is unclear whether chronic immunotherapy impacts relapse. As relapses are associated with worst outcome for certain forms of AIE, Reference Ariño, Armangué and Petit-Pedrol7 a better understanding of relapse and long-term management is crucial.
Given this, we reviewed all non-paraneoplastic AIE patients followed in the Calgary neuro-immunology clinic over 5 years, reporting on long-term management, relapse incidence and possible predictors of relapse within disease subtypes.
Methods
Study design and population
We performed a retrospective chart review consisting of all patients with antibody positive and antibody negative autoimmune encephalitis presenting to the Calgary Neuro-immunology Clinic and Tom Baker Cancer Centre between 2015 and 2020. Patients with paraneoplastic encephalitis, defined as those with encephalitis but an underlying neoplasm and antibody that could reasonably be associated with this neoplasm, were excluded due to difference in treatment response and prognosis. Reference Titulaer, McCracken and Gabilondo3,Reference Lancaster4 Patients that had history of neoplasm or current neoplasm for which the identified antibody did not have a clear association were included. Approval for the study was granted by the University of Calgary Co-joint Health Ethics Board. All variables were collected and assessed by the first author. The diagnosis of AIE was confirmed using recent consensus criteria, with all patients meeting criteria for at least probable AIE other than 3 patients which were possible AIE. Reference Graus, Titulaer and Balu8 These 3 possible AIE patients were antibody negative and either did not have CSF oligoclonal bands sent or did not have CSF studies available. All 3 patients had PET scans showing multifocal hypometabolism including the temporal lobes suggestive of possible autoimmune/inflammatory etiology.
Neural specific antibody testing for all patients was completed either through the Mayo Clinic and/or Mitogen Dx laboratories (Table 1). All patients had anti-neural antibody panels investigated through one of these labs, other than two NMDA encephalitis patients for which the location of their antibody testing was not available. There were 18 patients with testing sent to both Mitogen and Mayo laboratories. Dual testing was done to assess for antibodies not available at Mitogen laboratories in patients without an identified antibody, to confirm unexpected or discrepant results, or when an alternative lab was selected for repeat assessment later in the disease course. The encephalitis panels included antibodies against NMDAR, LGI1, VGKC, AMPAR, Caspr2 and GABA(B)R by cell based assay as well as paraneoplastic antibodies by immunoblot (amphiphysin, PNMA2 (Ma2/Ta), CV2.1, Ri, Recoverin, SOX1, Titin, Yo, Hu. In patients tested after 2019, antibodies against GAD65, Zinc4 and Tr were also included in the panel). Prior to 2019 GAD65 testing was done separately. In the patients with positive GAD65 antibodies, testing was done by line immunoassay for both patients as well as radioimmunoassay for one patient. Patients had either positive antibody in serum and CSF via line immunoassay or titers over 2,500 IU/ml documented.
Laboratory at which specimen (serum and/or CSF) was tested and serum and/or CSF antibody positivity results for various types of autoimmune encephalitis including LGI1 (n = 13), NMDA (9), antibody negative (8), GAD65 (2), GFAP (2), CASPR (2) and Hashimoto’s (2). Testing methodology included immunofluorescence, radioimmunoassay, or cell-based assay for samples sent to Mayo Clinic Laboratories and cell-based assay or line immunoassay for samples sent to Mitogen Dx Laboratories*

* GFAP antibody test not available through Mitogen Dx laboratories.
** Numbers include only patients with information regarding specimen type sent and result available on electronic medical record.
*** Positive serum TPO and Tg antibodies.
Demographic data, including age, sex, history of malignancy or current malignancy, comorbid autoimmune disorders, neuropsychiatric conditions and family history of these diseases, were collected. Clinical characteristics assessed were selected based on prior studies and diagnostic criteria. Reference Titulaer, McCracken and Gabilondo3,Reference Graus, Titulaer and Balu8 These included neurological, psychiatric and autonomic manifestations of AIE as well as disease severity necessitating ICU admission. Results of relevant investigations, including CSF studies, MRI, EEG and PET scan findings, were recorded. Collected data was used to calculate the Responsive-to-Immunotherapy-in-Epilepsy-and-Encephalopathy (RITE2) score. Reference Dubey, Singh and Britton9
Time to treatment and immunotherapy type, including acute treatment (intravenous and/or oral steroids, IVIg, PLEX) and chronic treatment (steroids, rituximab, cyclophosphamide, azathioprine, mycophenolate, methotrexate), as well as duration of treatment were documented. All time points were defined as time from symptom onset.
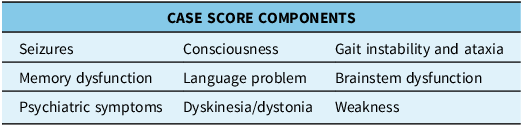
Relapse was defined as worsening neurological status reasonably attributable to AIE after at least 2 months of stability or improvement without other cause. Severity of relapse was determined using the Clinical Assessment Scale in Autoimmune Encephalitis (CASE) score Reference Lim, Lee and Moon10 (CASE score; Table 2). Collected variables were compared in relapsing VS non-relapsing groups as well as among relapsing patients. Subgroup analysis was completed for antibody positive, LGI1 and antibody negative AIE groups. Analysis of additional subgroups was not possible due to low number.
CASE score components used to evaluate presentation severity Reference Lim, Lee and Moon10

Statistical analysis
Statistical analyses were performed using VasserStats. All variables were assessed with descriptive analysis. Clinical and paraclinical categorical variables were converted to binary variables for purpose of analysis. Continuous variables were not modified for analysis. Possible predictors of relapse were assessed with the use of t-test for independent samples. A p-value of ≤ 0.05 was utilized for threshold of statistical significance.
Data availability
Anonymized data not published within this article will be made available by request from any qualified investigator.
Results
Patient characteristics
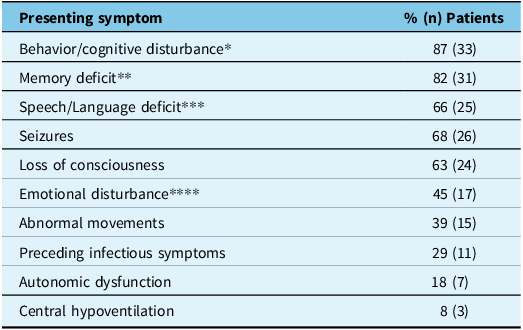
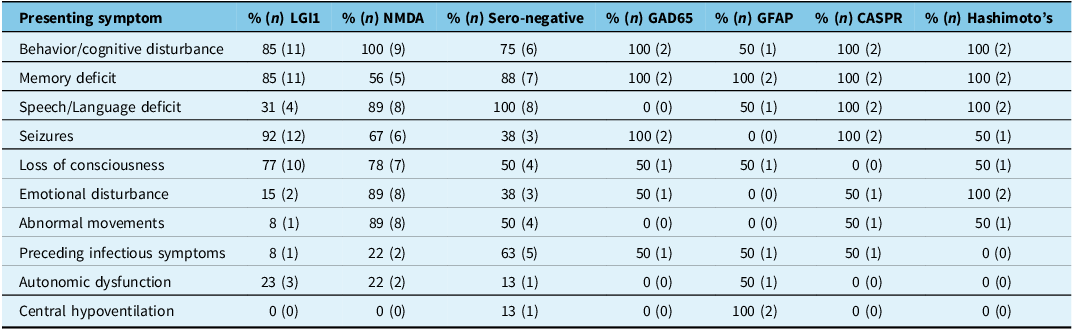
A total of 38 patients were included in analysis, 30 antibody positive and 8 antibody negative. The AIE subtypes included LGI1 (13), NMDA (9), Hashimoto’s (2), CASPR (2), GFAP (2), GAD65 (2) and antibody negative (8) encephalitis. All but one of the antibody negative encephalitis patients had testing at both Mitogen and Mayo laboratories. Of all the patients studied, the median age of onset was 61 years old (range 16–89). Median age was highest, 73 years old, in LGI1 AIE patients. Sixty-one percent (23/38) of patients were female. Common presenting symptoms (Table 3) included behavior or cognitive changes (87%; 33/38), memory deficits (82%; 31/38), speech or language disturbances (66%; 25/38) and seizures (68%; 26/38), which were focal onset in all cases where onset was known (85%; 22/26). Twenty-nine percent (11/38) of patients had preceding infectious symptoms. Dysautonomia was present in 18% (7/38) of patients and 21% (8/38) of patients required ICU admission. Reasons for ICU admission included seizure management, autonomic dysfunction and altered level of consciousness necessitating airway protection. This did not include patients requiring ICU admission due to treatment logistics such as PLEX administration. Initial presentation also varied by antibody type (Table 4). Mean initial CASE score was 6.4 (range 0–17).
Initial presenting symptoms in 38 patients with autoimmune encephalitis. Characteristics selected for assessment based on Titulaer et al., 2013 Reference Titulaer, McCracken and Gabilondo3

* Defined as psychotic symptoms and/or impairment of cognitive domains assessed by the Montreal Cognitive Assessment.
** Defined as any type of amnesia.
*** Defined as aphasia or language disturbance.
**** Defined as emotional instability or lack of emotional expression.
Initial presenting symptoms in patients with various types of autoimmune encephalitis including LGI1 (13), NMDA (9), antibody negative (8), GAD65 (2), GFAP (2), CASPR (2) and Hashimoto’s (2). Characteristics selected for assessment based on Titulaer et al., 2013 Reference Titulaer, McCracken and Gabilondo3

Investigations
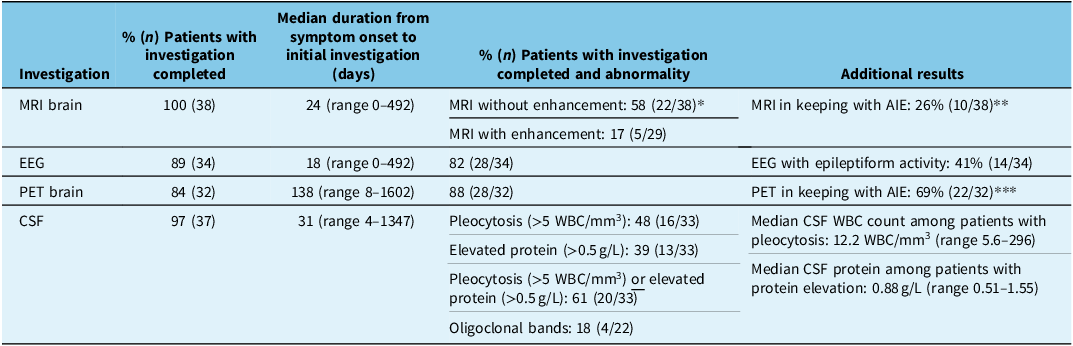
The majority of patients had at least one MRI, EEG, PET brain and CSF analysis completed. Table 5 contains further details including patients with investigatory results in keeping with AIE. Reference Graus, Titulaer and Balu8,Reference Bordonne, Chawki and Doyen11,Reference Quartuccio, Caobelli and Evangelista12
Investigation results for patients with various types of autoimmune encephalitis including LGI1 (13), NMDA (9), antibody negative (8), GAD65 (2), GFAP (2), CASPR (2) and Hashimoto’s (2)

* Temporal lobe most common location of abnormality.
** Defined as increased T2/FLAIR and/or increased diffusion signal in one or both mesial temporal lobes. Reference Ariño, Armangué and Petit-Pedrol7
*** Defined as temporal lobe hypometabolism or hypermetabolism. Reference Ariño, Armangué and Petit-Pedrol7,Reference Quartuccio, Caobelli and Evangelista12
Initial treatment
In regards to treatment, 36/38 patients received immunotherapy at some point in their disease course. The two untreated patients were LGI1 and antibody negative AIE, both had low initial CASE scores (2 and 1, respectively), and neither relapsed. Their lack of treatment did not have a statistically significant impact data analysis. Of treated patients, the duration of time from symptom onset to initial immunotherapy was a median of 43 days (range 4–987 days). Treatment delay was longest among the GAD65 AIE patients (median of 291 days; range 7–575 days) and shortest among the NMDA AIE patients (median of 30 days; range 4–581 days). Initial treatment included steroids (89%, 34/38 patients), IVIg (76%, 28/38 patients) and PLEX (20%, 7/38 patients). Fifty-five percent (21/38) of patients were put on a steroid sparing agent after initial presentation, 24% of these patients (5/21) had the agent initiated in the acute setting. When assessing type of steroid sparing agent initiated after initial presentation, azathioprine was the most used (57%, 12/21 patients), followed by rituximab (33%, 7/21 patients), and methotrexate (10%, 2/21 patients). For rituximab, 6 patients had the agent utilized as both second line immunotherapy as well as maintenance therapy; in contrast, azathioprine and methotrexate were initiated for maintenance therapy only.
Relapse
Patients were followed for a mean duration of 38.2 months, with the range being 3.0–103.1 months. Outcome data of relapse was available in 37/38 patients (see appendix table 1.0). Seventeen of thirty-seven (46%) patients relapsed during this time. Specifically, 6/9 (67%) NMDA, 6/12 (50%) LGI1, 1/2 (50%) Hashimoto’s, 1/2 (50%) CASPR, 2/8 (25%) antibody negative, 1/2 (50%) GAD65 and 0/2 (0%) GFAP encephalitis patients relapsed. The median time to relapse was 16.3 months (range 2.4–63.1 months), and 76% (13/17) of the relapsing patients had their first relapse within 3 years. In terms of clinical presentation and investigatory results, there was no significant difference in age, sex, initial CASE score, RITE score, prevalence of abnormal EEG or CSF between the relapsing and non-relapsing groups. However, when analyzing only the AIE subtypes with neural antibodies against cell surface/synaptic targets (NMDAR, LGI1, CASPR2), those with abnormal CSF were more likely to relapse (p = 0.037).
When comparing initial treatment in relapsing VS non-relapsing groups, there was no significant difference in duration from symptom onset to treatment initiation between groups (p = 0.081), nor was there a significant difference in initial treatment with IV VS oral steroids or combination treatment with steroids plus IVIg or PLEX VS steroids, IVIg, or PLEX alone. Furthermore, there was no difference in steroid or steroid sparing treatment use at 3, 6 and 12 months after initial presentation between the relapsing and non-relapsing groups. At the time of relapse, 10/17 (58.5%) of relapsing patients were on immunotherapy. This included steroids (53%, 9/17 patients), IVIg (6%, 1/17 patients) and azathioprine (18%, 3/17 patients). Patients were on azathioprine for a mean of 175 days (range of 43–427 days) prior to relapse. Six of seventeen (35%) of relapsing patients had a recent (<30 days) immunotherapy dose decrease prior to relapse.
When looking at relapse severity, overall patients had lower mean CASE scores at relapse compared to initial presentation (5.18 vs 6.53; p = 0.040). Relapsing patients initiated on immunotherapy at or before 6 months and 12 months from initial presentation had lower CASE scores at relapse compared to those not on treatment at these time points, however this did not reach statistical significance (CASE score = 4 vs 5.75, p = 0.085; CASE score = 3.67 vs 6, p = 0.056; Figure 1). Additionally, patients on any immunotherapy at the time of relapse, had less of an increase in CASE score at relapse compared to those not on immunotherapy at the time of relapse (ΔCASE score = 1.3 vs 4.6, p = 0.0035; Figure 1).
(a) CASE score at relapse for patients on VS not on immunotherapy at 6 months (CASE = 4.0 vs 5.75; p = 0.085) and 12 months (CASE = 3.67 vs 6.0; p = 0.056) (b) Increase in CASE score at relapse (CASE Scorerelapse – CASE Scorepre-relapse) for patients on VS not on immunotherapy at time of relapse (ΔCASE Score = 1.3 vs 4.6; p = 0.0035).

Individual analysis of the LGI1 group did not reveal additional significant differences between relapsing and non-relapsing groups. Individual analysis of the antibody negative group revealed seizures were more common in the non-relapsing group (67% vs 0%; 4/6 patients vs 0/6 patients; p = 0.033), however there was no significant difference in the remainder of the clinical presentation between relapsing and non-relapsing groups. Subgroup analysis of the remaining AIE groups was not possible due to low number.
Regarding management of relapse, a new immunotherapy or treatment modification was initiated at relapse in all relapsing patients (17/17). The delay from relapse symptom onset to treatment initiation was a median of 11 days (range 0–87 days), significantly shorter than initial presentation (p = 0.0014). The most common acute treatments used at relapse were steroids (88%, 15/17) and IVIg (76%, 13/17). Following relapse, 15/17 (88%) of patients were on a steroid sparing agent with the most common being rituximab (59%, 10/17), followed by azathioprine (29%, 5/17).
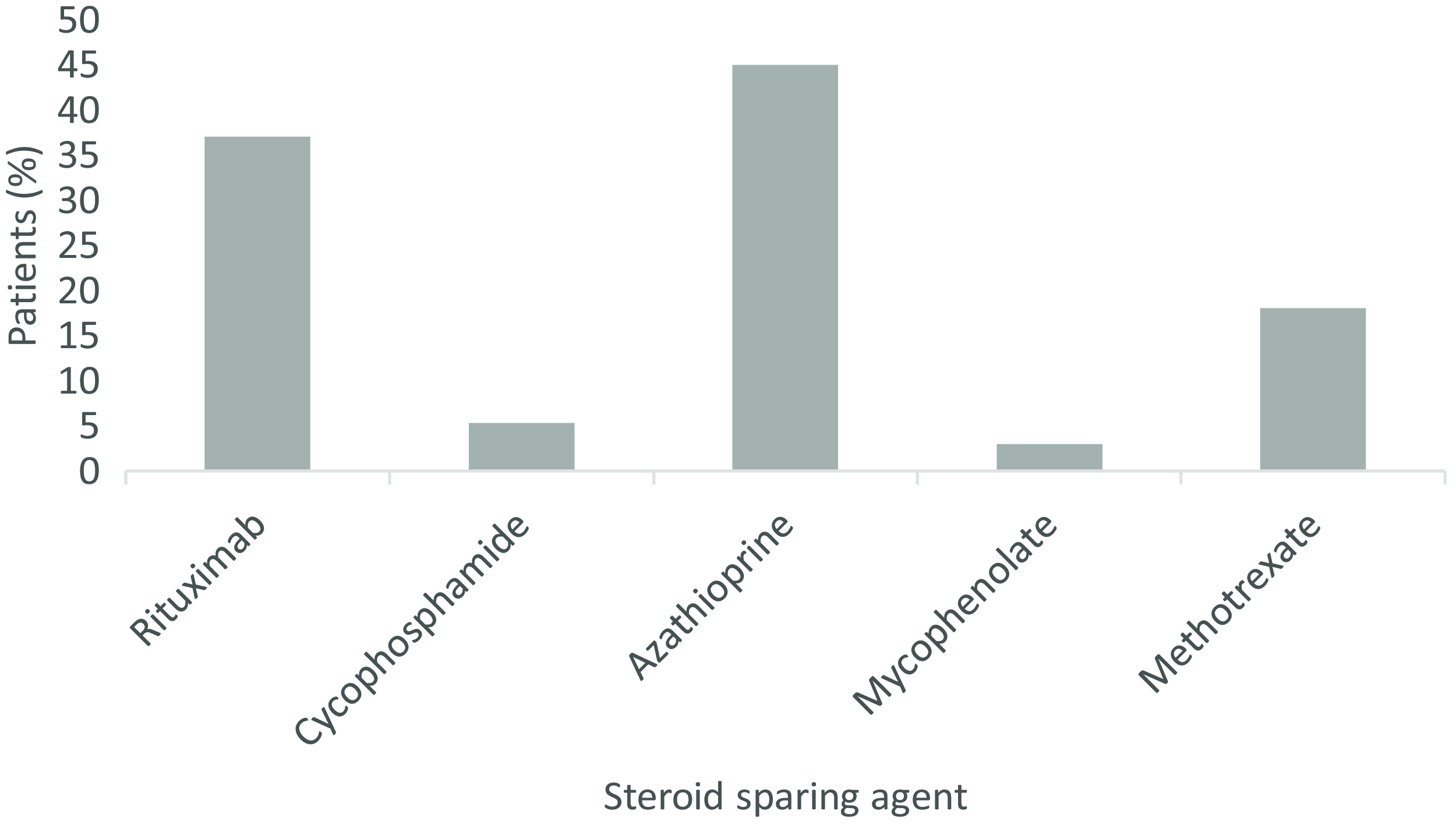
Looking at all patients throughout the follow-up period, 68% (26/38) were treated with some combination of steroids plus IVIg and/or PLEX, with 32% (12/38) of these treated with steroids plus both IVIg and PLEX. A combination of steroids plus a steroid sparing agent was used in 58% (22/38) of patients. Overall, 76% (29/38) of patients were initiated on a steroid sparing agent at some point during their disease course. Azathioprine was the most used (45%, 17/38), others included rituximab (37%, 14/38), methotrexate (18%, 7/38), cyclophosphamide (5%, 2/38) and mycophenolate (3%, 1/38) (Figure 2).
Percent of patients treated with various steroid sparing agents throughout disease course including rituximab (37%), cyclophosphamide (5%), azathioprine (45%), mycophenolate (3%) and methotrexate (18%).

Discussion
This study describes our single-center experience in long-term follow-up and chronic management of AIE with a mean follow-up of over 3 years (range of 3.0–103.1 months). In this time period, relapse was not infrequent for various subtypes of AIE, despite the majority (55%) of our patients being on a steroid sparing agent or chronic immunotherapy after diagnosis. Specifically, relapse ranged from 0% in GFAP antibody positive patients up to 67% in NMDA antibody positive patients. Relapse typically occurred within the first 3 years after initial presentation, although 24% of patients relapsed even beyond 3 years.
No definitive predictors of relapse were found in our patients. Possible predictors of relapse included the CSF abnormalities of pleocytosis and elevated protein, although this was statistically significant only in patients with typical cell surface antibodies (NMDA, LGI1, CASPR). Literature on the implication of abnormal CSF results is inconclusive. Reference Gabilondo, Saiz and Galan17,Reference Zeng, Cao, Zheng and Yu18 Antibody titers were not available for comparison in our patients; however, some studies suggest rising CSF antibody titers and persistently elevated oligoclonal bands may be predictive of impending relapse. Reference Abboud, Probasco and Irani5,Reference Zeng, Cao, Zheng and Yu18 Furthermore, recent literature suggests increased neurofilament light chain levels in the CSF may indicate and predict severity of inflammatory CNS diseases. Reference Guasp, Martín-Aguilar and Sabater19 The clinical practicality of repetitively pursuing lumbar punctures to monitor disease state is questionable. Antibody positivity can persist even after disease recovery Reference Lee, Lee and Kim6,Reference Zeng, Cao, Zheng and Yu18 and are, of course, not useful for monitoring antibody negative disease.
Investigations completed were in line with consensus recommendations with almost all patients having MRI and CSF studies (100%, 97% respectively) and most having confirmed paired CSF/serum neural antibody testing (76%). Reference Abboud, Probasco and Irani5 Initial treatment of our patients was also in keeping with recent consensus recommendations on acute therapy Reference Abboud, Probasco and Irani5 with all but two patients receiving some combination of IVIg, steroids and/or PLEX. Interestingly, in our cohort the type of acute treatment did not appear to impact relapse. Initial treatment with oral VS IV steroids did not differ between relapsing and non-relapsing groups, nor did initial treatment with a combination of steroids plus IVIg or PLEX VS steroids, IVIg, or PLEX alone. Literature on optimal acute therapy is limited, however some evidence suggests initial combination treatment with steroids plus IVIg may be associated with better outcome when compared to either treatment alone. Reference Shin, Lee and Shin22 Rituximab use in our group was less common than some of the other steroid sparing agents (37% of all patients on steroid sparing therapy) and may relate to provincial funding restrictions for this medication.
We did not provide further evidence that early initiation of immunotherapy significantly reduces relapse occurrence, although this is well documented in prior studies. Reference Titulaer, McCracken and Gabilondo3,Reference Abboud, Probasco and Irani5,Reference Lee, Lee and Kim6,Reference Nosadini, Mohammad, Ramanathan, Brilot and Dale13,Reference Thaler, Zimmermann and Kammermeier15,Reference Van Coevorden-Hameete, Wirtz, Schreurs, Sillevis Smitt and Titulaer20,Reference Uy, Binks and Irani21 This may be due to the relatively quick initiation of initial treatment in our patients overall, as well as small sample size and disease heterogeneity. The median delay from initial symptom onset to treatment in our patients was 43 days, shorter than in other studies. Reference Smith, Dubey, Liebo, Flanagan and Britton14,Reference Van Coevorden-Hameete, Wirtz, Schreurs, Sillevis Smitt and Titulaer20 Within our study patients however, relapsing patients had significantly earlier initiation of immunotherapy along with a less severe presentation at relapse compared to initial presentation. This suggests that earlier initiation of treatment may prevent progression of disease, leading to less severe disease nadir. In addition, patients on immunotherapy at the time of relapse had milder relapses as reflected by their CASE scores. Although we cannot infer from our results a difference in efficacy between steroids and steroid sparing agents, our results suggest being on any form of immunotherapy at relapse reduces relapse severity. Other studies have suggested steroid sparing treatment also reduces overall relapse risk; Reference Abboud, Probasco and Irani5,Reference Nosadini, Mohammad, Ramanathan, Brilot and Dale13,Reference Smith, Dubey, Liebo, Flanagan and Britton14,Reference Zeng, Cao, Zheng and Yu18 however, we did not provide further evidence for this. This may be due to the number of patients in our study as well as the type of steroid sparing agent used in our patient population. As above, most of our patients were preferentially initiated on azathioprine. However, rituximab was more commonly used in other studies, Reference Abboud, Probasco and Irani5,Reference Thaler, Zimmermann and Kammermeier15,Reference Uy, Binks and Irani21,Reference Shin, Lee and Park23 which may be more efficacious than other steroid sparing agents. Reference Abboud, Probasco and Irani5,Reference Thaler, Zimmermann and Kammermeier15,Reference Uy, Binks and Irani21
Currently the Autoimmune Encephalitis Alliance recommends that long-term immunotherapy decisions should be based both on the severity of initial attack and the risk of relapse, Reference Abboud, Probasco and Irani5 which, particularly for antibody negative AIE, is lacking data. The suggested approach is to start long-term immunotherapy after the second attack unless the first presentation is severe, or the patient has additional risk factors for relapse. Reference Abboud, Probasco and Irani5 The optimal duration of immunotherapy is unknown. Prior studies, specifically for anti-NMDAR encephalitis, have suggested a duration ranging from 1 to 3 years; Reference Titulaer, McCracken and Gabilondo3,Reference Dalmau, Lancaster and Martinez-Hernandez24 however, these timelines lack strong supportive evidence. For antibody negative patients, recent evidence suggests the continuation of immunotherapy is associated with more improvement; however, the effect beyond 12 months is unknown. Reference Lee, Lee and Kim6
The risk benefit ratio of chronic immunotherapy in AIE remains unclear. Chronic treatment may have benefit in reducing relapse severity, although we did not specifically assess whether this effects long-term clinical outcome. Nonetheless, the risk of chronic continued immunotherapy is likely not insubstantial when considering that relapse can occur more than 3 years after initial presentation in a minority. Accordingly, long-term follow-up and disease monitoring is important and decisions around initiating chronic immunotherapy should factor in the severity of initial presentation as well as patient factors which may influence risk of immunosuppression. Reference Abboud, Probasco and Irani5
A major limitation to our study and interpretation of relapse predictors is the collective analysis of various AIE subtypes. As we gain further insight into the pathophysiology and presentation of the different antibody syndromes it seems likely that they will be increasingly treated as distinct diseases under the umbrella term of AIE, similar to the distinction between multiple sclerosis and neuromyelitis optica syndrome under the umbrella of “demyelinating diseases.” While the objective of describing long-term management and relapse incidence was possible for the AIE subtypes, further subgroup analysis was limited due to a low number in each subtype. Nonetheless, this provides important information on the “real-world” follow-up of heterogenous AIE patients in a dedicated autoimmune neurology clinic and the need for long-term monitoring due to ongoing risk of relapse.
A further limitation is the retrospective nature of the chart review, leading to variation in the quantity and quality of data available for each patient. Specifically, there was variation in the laboratory that patients had their CSF studies completed at. This prevented the quantitative comparison of antibody titers and oligoclonal bands, which may have provided further insight into predictors of relapse and monitoring of treatment response. Reference Zeng, Cao, Zheng and Yu18 Additionally, the Mitogen Dx neural antibody panel used to evaluate many of our patient’s antibody status does not include some neural antibodies (e.g. anti-GFAP, KLHL11) and lacks a complementary tissue-based assay to more comprehensively screen for anti-neural antibodies. While all but one antibody negative patient also had testing completed at the Mayo clinic laboratories, there is growing literature suggesting misdiagnosis of antibody negative AIE in patients with antibodies not included in standard diagnostics panels. Reference Dalmau and Graus25 Thus, it is likely that some of the antibody negative patients were antibody positive for a less common antibody given the narrow subset of testing done for some patients. Neural antibody testing with incorporation of a tissue-based assay to screen for novel/rarer antibodies, like is employed by the Mayo Clinic, is therefore essential to maximize sensitivity and specificity of this testing. Reference Budhram, Yang, Bhayana, Mills and Dubey26 Finally, the steroid sparing agent most used in our patients, azathioprine, may be less efficacious than other agents, namely rituximab, which is more commonly used in other studies. As a result, the impact of steroid sparing agents, in general, on relapse may have been underestimated.
Conclusion
This single-center experience demonstrates that relapse risk is high for various subtypes of AIE and provides evidence for the need of longitudinal follow-up of patients, which in our study allowed for earlier treatment initiation and less severe relapses compared to initial presentation. It is challenging to comment on relapse predictors as the lower number of patients restricted our subgroup analysis, but this represents an important area of need for additional research in AIE.
Current consensus recommendations suggest initiating steroid sparing treatments after first relapse unless the patient has a severe initial presentation or additional risk factors for relapse. Reference Abboud, Probasco and Irani5,Reference Nosadini, Mohammad, Ramanathan, Brilot and Dale13 There is limited guidance surrounding duration of immunotherapy after initial presentation. Our patients who were on immunotherapy at the time of relapse did have milder relapses although their overall risk of relapse was not lower than those not on chronic treatment. However, this may be a reflection of the type of immunotherapy used and a limitation of the lower number of patients in our study.
Overall the clinical risk/benefit ratio of chronic immunotherapy in the context of lessening the burden of, or even preventing, a single relapse in 3 years is unclear. Our data enforce the importance of long-term follow-up, allowing for close monitoring, and the need for identification of further predictors of relapse. Without such predictors, it remains challenging to best select patients that would most benefit from the initiation and continuous use of immunotherapy after initial presentation.
Supplementary material
The supplementary material for this article can be found at https://doi.org/10.1017/cjn.2024.278.
Acknowledgements
The authors thank the patients for their participation and all referring physicians.
Author contributions
MH collected the data, completed the statistical analysis and created all figures and tables. MH and CH drafted the initial version of the manuscript. RK, KA and PD participated in revisions of the manuscript.
Funding statement
None.
Competing interests
None.